Die Sicherheitstechnische Kontrolle (STK) ist eine für Betreiber von Medizinprodukten vorgeschriebene periodische Sicherheitsüberprüfung. In der Medizintechnik ist die STK eine Maßnahme zur Feststellung der Sicherheit eines aktiven, nichtimplantierbaren Medizinproduktes.Das Ziel dieser Maßnahme ist das rechtzeitige Erkennen von Gerätemängeln und Risiken für Patienten, Anwender oder Dritte.. Messtechnische Kontrollen medizinischer Geräte. In der MPBetreibV wird außerdem vorgegeben, für welche medizinischen Messgeräte eine messtechnische Kontrolle (MTK) verpflichtend ist. In Anlage 2 werden alle MTK-pflichtigen Geräte aufgeführt, wie beispielsweise Ergometer oder Blutdruckmessgeräte.Ähnlich wie bei der STK ist für die MTK ebenfalls vorgeschrieben, dass nur Fachpersonen.

Innovative Materialien in Medizinprodukten Wissensplattform nanopartikel.info

Welche Kontrollen gibt es bei Medizinprodukten?

Biokompatibilität bei Medizinprodukten qtecgroup

Gesundheit Medizin Immer mehr fehlerhafte Implantate Südwest Presse Online

Klinische Bewertung von Medizinprodukten Darauf kommt es an
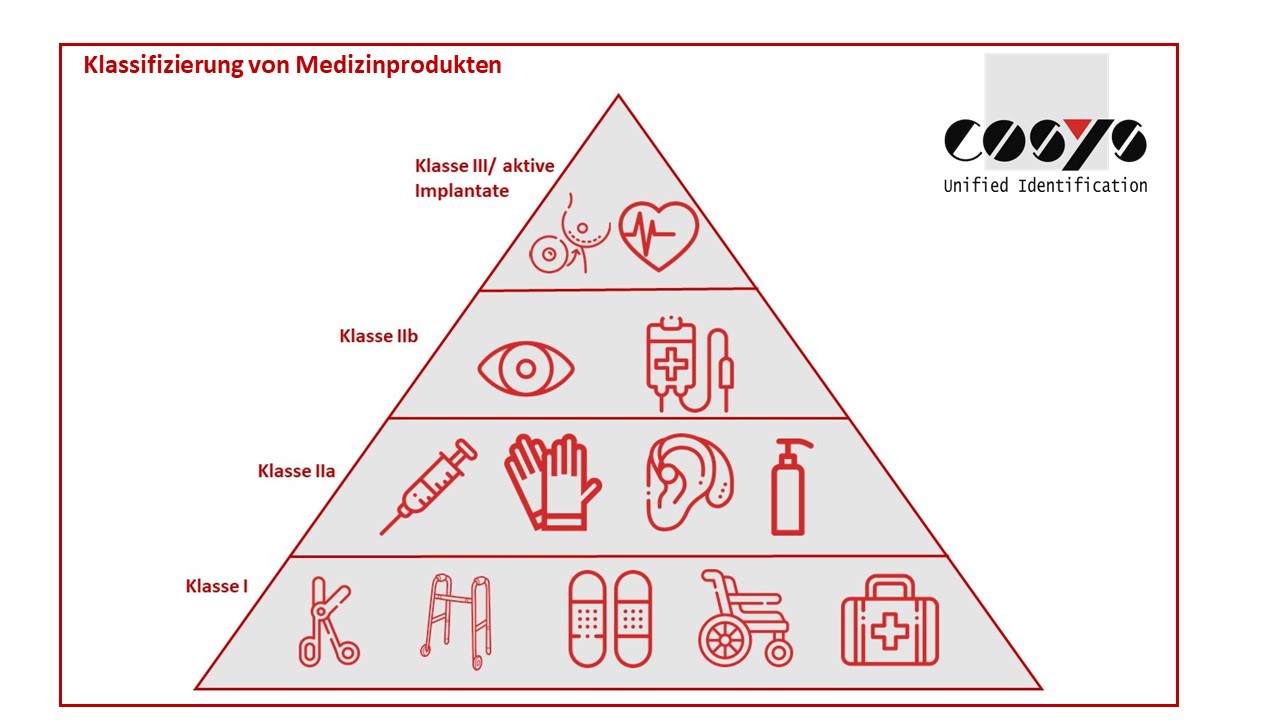
Medical Device Regulation MDR
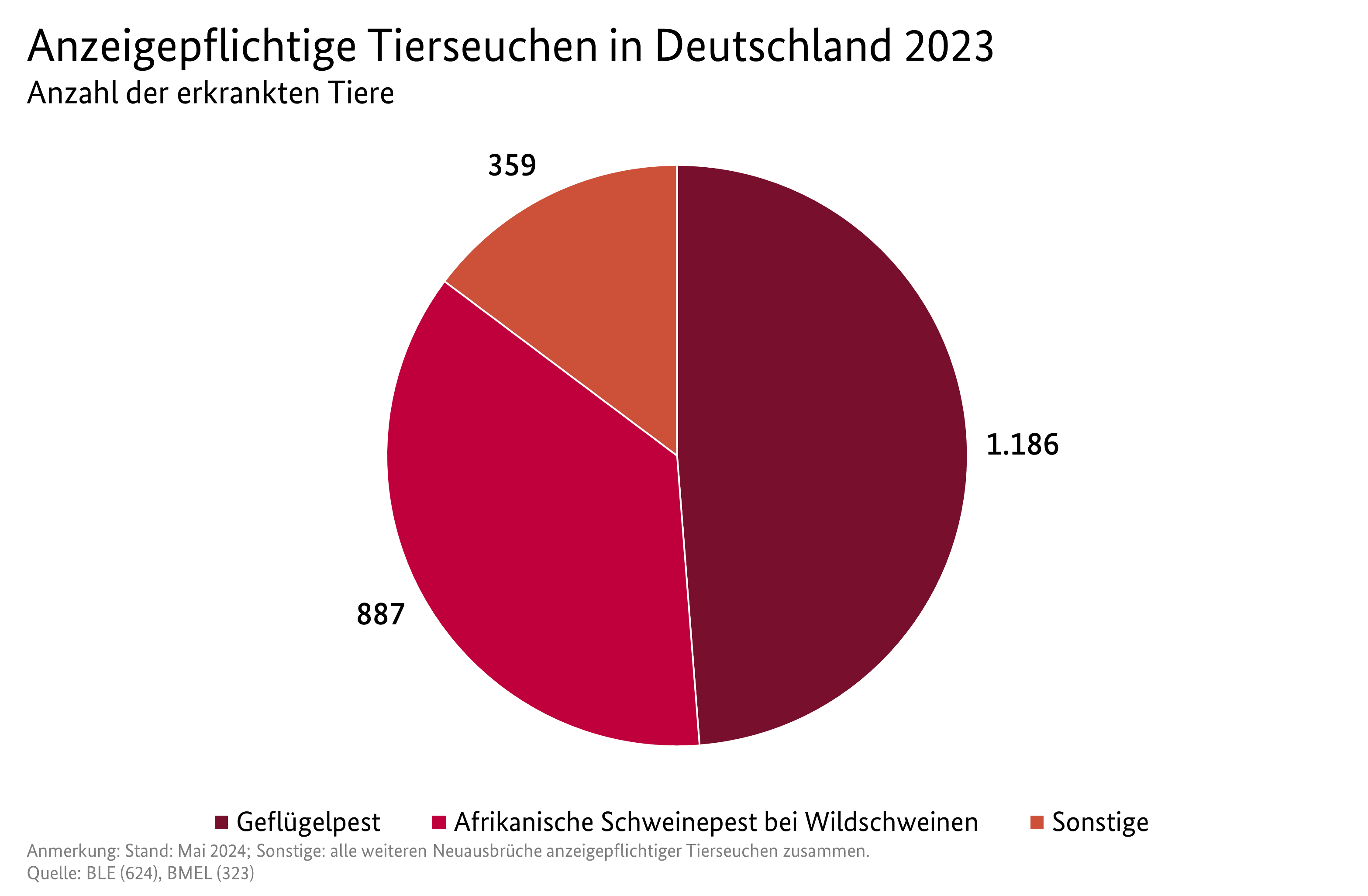
BMELStatistik Veterinärwesen

Meditec Source Medizinprodukte Aufbereitung valide dokumentieren
Gefahr durch Angriffe Herzschrittmacher und Insulinpumpen von Hackern angreifbar

Welche informationen liefern Blutdruckgeräte?

CoronaSchnelltests Wer kann eine Teststelle eröffnen?
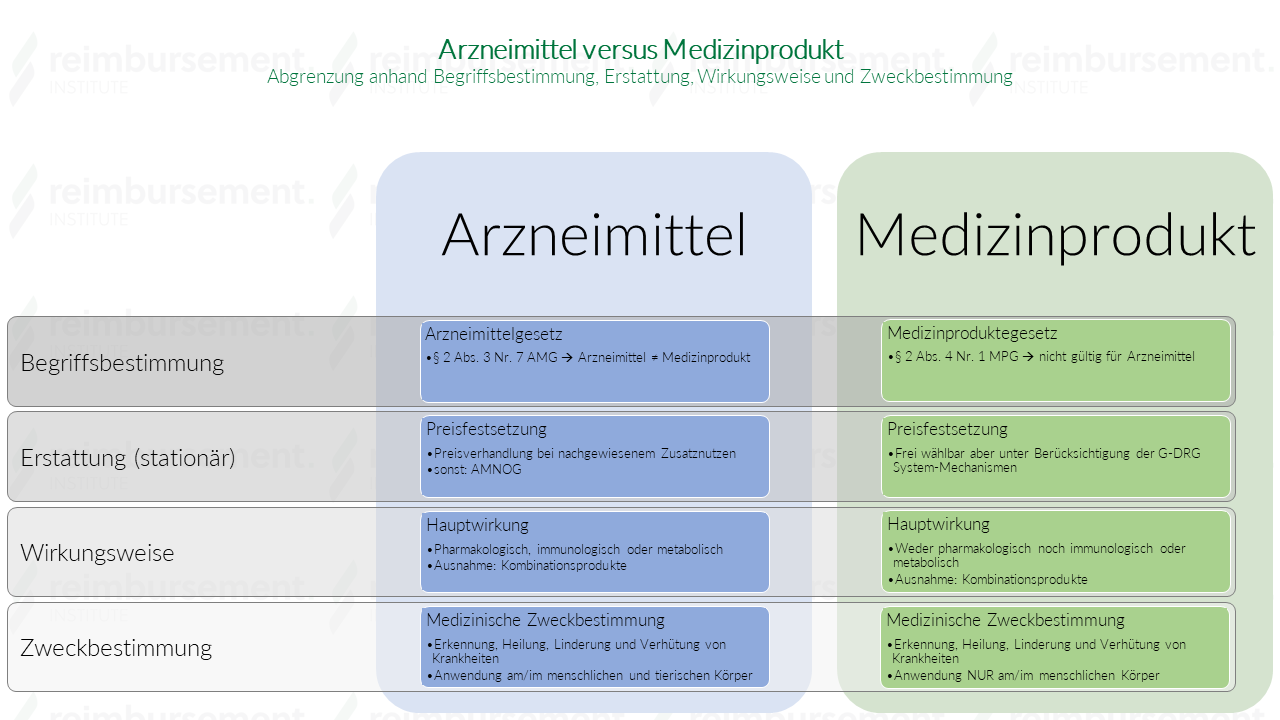
Arzneimittel versus Medizinprodukt

Digitaler Postausgang Briefe einfach elektronisch versenden

Medizinprodukt Definition, Kriterien zur Klassifizierung, Risikoklassen

Haftungsrecht Vorsicht bei der Eigenherstellung von Medizinprodukten

Eindeutige Kennzeichnung von Medizinprodukten

Screenshot_Lieferantenbewertung QEnthusiast Das neue Qualitätsmanagement

Grüner Knopf Neues Siegel für nachhaltige Kleidung YouTube
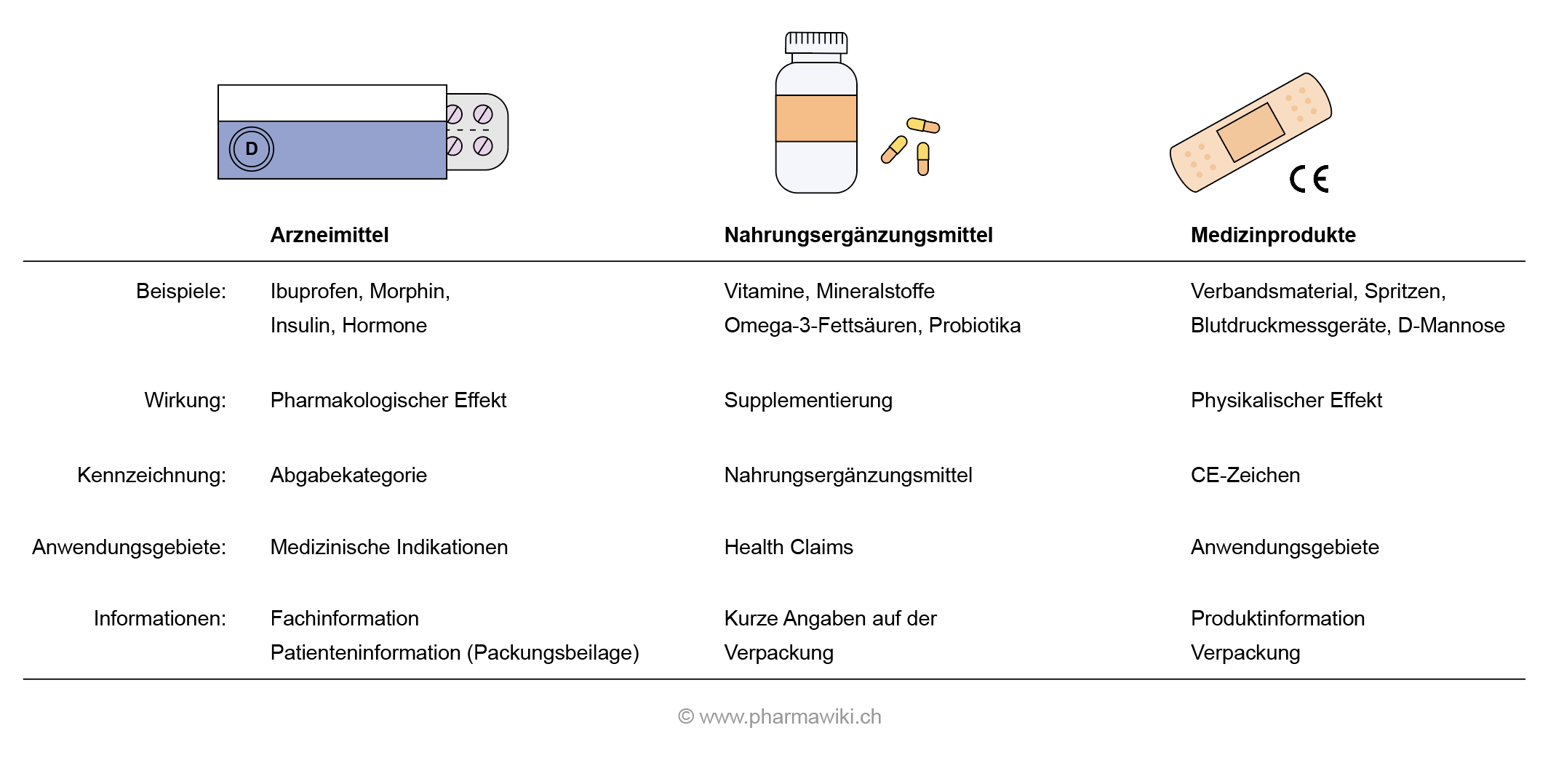
Unterschied Medizinprodukt Und Arzneimittel

Lieferengpässe bei Medizinprodukten in Kliniken MDR THÜRINGEN JOURNAL MDR YouTube
Es gibt drei Arten von klinischen Prüfungen, für die die Anforderungen der MDR gelten: Klinische Prüfungen für die Konformitätsbewertung (Typ A) nach Art. 62 sind genehmigungspflichtig. Es gelten die Art. 62 bis 81 und die Anforderungen des Anhangs XV. Klinische Prüfungen im Rahmen vom Post-Market Clinical Follow-Up (PMCF, Typ C) sind.. Wie vielleicht bereits deutlich geworden ist, muss bei Medizinprodukten sowohl die Verifikation als auch die Validierung erfolgen. Es gibt einige wenige Ausnahmefälle, in denen sich Produkte nicht so einfach verifizieren lassen. Dann besteht immer noch die Möglichkeit, den Entstehungsprozess des Produktes zu validieren.


